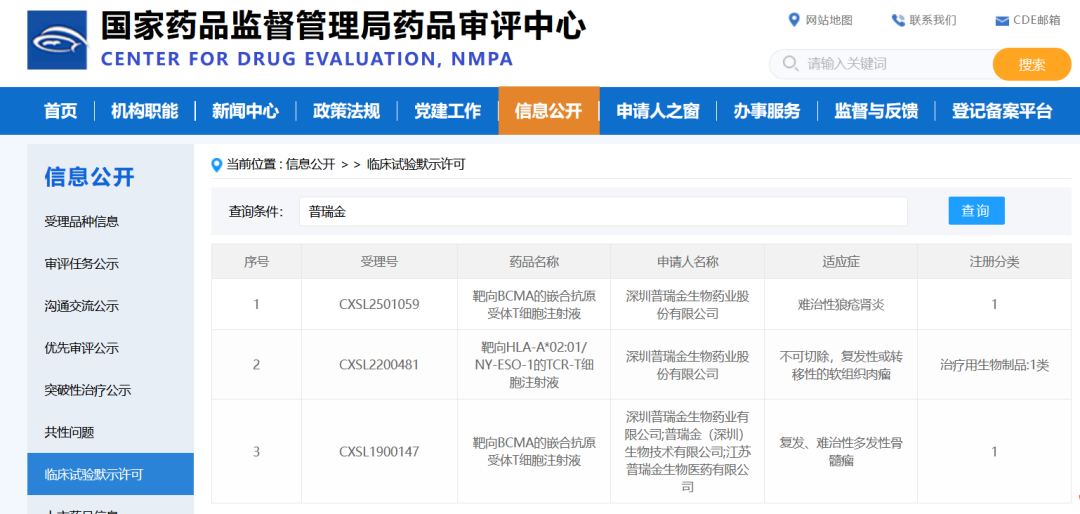
近日,據國家藥品監督管理局藥品審評中心(CDE)官網顯示,深圳普瑞金生物藥業股份有限公司(以下簡稱“普瑞金”)自主研發的"靶向BCMA的嵌合抗原受體T細胞注射液",在復發、難治性多發性骨髓瘤適應癥臨床試驗推進的同時,申請的新適應癥已正式獲得臨床試驗批準通知書,新適應癥為難治性狼瘡腎炎。
狼瘡腎炎的根源是系統性紅斑狼瘡(SLE,常簡稱為"狼瘡"),是SLE引發的腎臟損害,伴腎小球足細胞、腎小管間質或腎血管病變,屬嚴重疾病。美國權威政府衛生機構—國家糖尿病、消化和腎臟疾病研究所(NIDDK)指出,在SLE的成年患者中,多達50%的人會出現腎損害臨床表現;在臨床上,經腎組織病理檢查發現腎臟病變者更是高達90%。
在細胞治療產品拓展新適應癥的過程中,申報策略和工藝變更尤為重要。"靶向BCMA的嵌合抗原受體T細胞注射液"從復發、難治性多發性骨髓瘤到難治性狼瘡腎炎的跨越,是從血液腫瘤到自身免疫病的轉變。
萊恩醫藥是國際化的生物醫藥產品非臨床研究和評價平臺,研究數據已被美國、歐盟等多個發達國家和地區監管機構認可,可支持全球申報。作為“廣東省高水平新型研發機構”,憑借“廣東省藥物非臨床評價與研究重點實驗室”、“廣東省創新藥物評價與研究工程技術研究中心”、“廣東省細胞與基因治療創新藥物工程技術研究中心”等研究平臺及既往成功申報的研究經驗,針對“靶向BCMA嵌合抗原受體T細胞注射液”新適應癥的臨床轉化需求,為其制定了精準的申報策略,并開展了工藝變更后的橋接非臨床研究,助力項目獲得臨床試驗默示許可,萊恩醫藥特在此祝賀合作伙伴普瑞金取得新的成就!
關于普瑞金
深圳普瑞金生物藥業股份有限公司為國家高新技術企業、廣東省細胞與基因治療創新藥物工程技術研究中心、深圳市專精特新企業,投資方股東包括國家中小企業發展基金、國科嘉和、海爾資本、深圳資本集團、華邦健康(002004)等。多年深耕于細胞與基因治療藥物領域,產品管線包括多個靶點的CAR-T、CAR-NK藥物等,適應癥涵蓋血液系統腫瘤、實體瘤和自身免疫疾病等多個治療領域。普瑞金堅持技術平臺化、平臺產品化、產品商業化、商業國際化的發展策略和道路,是目前業內率先實現CAR-T細胞藥物全球多區域授權的領先創新細胞藥物企業。經過多年投入和發展,普瑞金已經建立了完整的細胞藥物研發和生產質量管理體系,成功搭建了納米抗體篩選、免疫細胞藥物發現、質粒/病毒載體工藝開發和生產、細胞工藝開發和生產的創新和產業化核心技術平臺,通過了ISO9001質量管理體系認證。